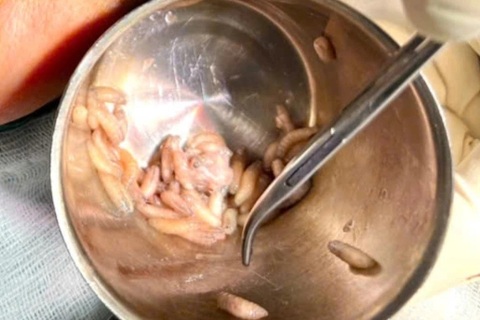
VN Pharma đã “khoác áo” Canada cho lô thuốc chữa ung thư H-Capita như thế nào?
(Dân trí) - Cơ quan chức năng xác định, 9.300 hộp H-Capita 500mg Caplet có nguồn gốc xuất xứ từ Ấn Độ nhưng Công ty Cổ phần VN Pharma (CPVNPM) đã dùng thủ đoạn làm giả các giấy tờ để “khoác áo” Canada cho lô thuốc này khi xin cấp phép nhập khẩu.
Theo Thanh tra Chính phủ (TTCP), qua báo cáo của Bộ Y tế cũng như các tài liệu đã được Cục quản lý Dược bang Himachal và Bộ nội vụ bang Himachal, Ấn Độ, Bộ Ngoại giao Ấn Độ, Đại sứ quán Việt Nam tại Ấn Độ xác nhận thì lô thuốc 9.300 hộp H-Capita mà VN Pharma làm thủ tục nhập khẩu về Việt Nam do nhà máy Affy Parenterals của Ấn Độ sản xuất ngày 5/3/2014, lô số CTP0314B1 (WHO/GMP), hạn sử dụng 4/4/2016. Phiếu kiểm tra xuất xưởng ngày 05/3/2014 xác định lô thuốc đạt các tiêu chuẩn sản xuất, trong đó: hàm lượng hoạt chất chính Capecitabine đạt 99,54%, hàm lượng tạp chất không định danh 0,048%.
Số thuốc này Công ty Affy Parenterals bán cho Công ty Magnolia limited (địa chỉ 11/621, Sai-Krupa Bldg. Pum Bhiwandi, Thane, Ấn Độ), Công ty Magnolia limited lại bán lại cho Công ty CPVNPM thông qua công ty lấy tên là Helix Pharmaceuticals Inc., đia chỉ ghi trên giấy tờ ghi là 392 Wilson Avenus, Toronto, Ontario, Canada. Số thuốc này được vận chuyển đến Singapore, rồi làm thủ tục thông quan tại Sân bay Tân Sơn Nhất. Ngày 11/4/2014, Công ty CPVNPM lập Tờ khai hải quan số 6520 đề nghị và được Hải quan cửa khẩu Tân Sơn Nhất cho phép nhập khẩu 9.300 hộp thuốc H-Capita vào Việt Nam ngày 11/4/2014.
Bất thường trong việc đấu thầu nên bị… lộ
Thanh tra Chính phủ cũng cho hay, Công ty CPVNPM năm 2014 tham gia đấu thầu thuốc tại Bệnh viện Đại học Y dược TPHCM, trong danh mục thuốc trúng thầu có 15.000 viên thuốc H-Capita 500mg Caplet của Công ty Helix Pharmaceuticals Inc., Canada sản xuất; đơn giá 37.000 đồng/viên với tổng giá trị 555 triệu đồng.
Công ty TNHH MTV Dược Nam Anh (Chủ sở hữu là Công ty CPVNPM) năm 2014 cũng tham gia đấu thầu và trúng thầu 46 mặt hàng thuốc tại Sở Y tế TPHCM, trong đó có mặt hàng thuốc H-Capital (thuộc nhóm 1). Nhà thầu Nam Anh đã ký hợp đồng cung ứng thuốc cho các cơ sở y tế, riêng thuốc H-Capita 500mg Caplet ký hợp đồng với số lượng 471.275 viên với 4 bệnh viện (BV Nguyễn Tri Phương 20.000 viên; BV Nhân dân Gia Định 10.000 viên; BV Bình dân Gia Định 100.000 viên; BV Trưng Vương 341.275 viên). Đơn giá thuốc H-Capita 500mg trúng thầu là 31.000 đồng/viên, bằng 47% đơn giá kế hoạch đấu thầu thuốc của Sở Y tế TPHCM và bằng 60% đơn giá các thuốc có cùng hoạt chất Capecitabine 500mg thuộc thuốc Nhóm 1 khác trúng thầu năm 2014 tại các địa phương. Đơn giá thuốc này tương đương đơn giá thuốc có cùng hoạt chất Capecitabine 500mg thuộc nhóm 2 và đơn giá thuốc do Ấn Độ sản xuất.
Cục Quản lý dược (QLD) sau khi xem xét lại giá kê khai và giá trúng thầu thuốc H-Capita 500mg tại Hội đồng đấu thầu thuốc Sở Y tế TPHCM thấy giá thuốc H-Capita của Công ty Dược Nam Anh trúng thầu thấp hơn nhiều so với giá trúng thầu thuốc cùng loại được sản xuất từ các nước thuộc hệ thống hợp tác về thanh tra trong lĩnh vực thực hành tốt sản xuất thuốc mà Canada là một thành viên. Cục QLD đã yêu cầu Công ty CPVNPM giải trình về đơn giá trúng thầu, đồng thời yêu cầu Công ty tạm ngừng việc nhập khẩu, lưu hành thuốc H-Capita 500mg.
Cục QLD đã phối hợp với cơ quan An ninh điều tra – Bộ Công an, Cục Lãnh sự Bộ Ngoại giao, Bộ Y tế Canada và Đại sứ quán Canada tại Việt Nam để xác minh làm rõ các thông tin liên quan. Các cơ quan này đã xác định nội dung hợp pháp hóa lãnh sự trên giấy tờ của Công ty Helix Pharmaceuticals Inc, Canada là giả mạo và không có Công ty Helix Pharmaceuticals Inc tại địa chỉ được ghi trong giấy chứng nhận bán hàng tự do (FSC), giấy chứng nhận thực hành tốt sản xuất thuốc (GMP).
Kết luận của Thanh tra Chính phủ xác định, khi phát hiện vi phạm liên quan đến hồ sơ hành chính của thuốc H-Capita, Cục Quản lý Dược đã kịp thời niêm phong lô thuốc không cho lưu hành ra thị trưởng, gửi văn bản đến cơ quan công an để điều tra; thu hồi số đăng ký 7 thuốc, thu hồi giấy phép nhập khẩu 3 thuốc ((H-Capita, H-Epra 40 và H-Lastapen 500mg) song Cục Quản lý Dược và các đơn vị, cá nhân liên quan chịu trách nhiệm trực tiếp về những thiếu sót, vi phạm.
Thanh tra Chính phủ kiến nghị Bộ Y tế chỉ đạo Cục Quản lý Dược và Vụ Kế hoạch – Tài chính tổ chức kiểm điểm và có biện pháp xử lý đối với tập thể, cá nhân có liên quan để xảy ra những vi phạm trong việc cấp phép nhập khẩu, cấp số đăng ký đối với 10 thuốc, cấp phép hoạt động cho Công ty Helix năm 2014. Đồng thời có biện pháp xử lý đối với tập thể, cá nhân có liên quan đến việc cho phép nhập khẩu 9.300 hộp thuốc H-Capita Caplet 500mg vào Việt Nam.
Mặc dù hồ sơ, tài liệu bị làm giả song Thanh tra Chính phủ cho rằng, Hội đồng tư vấn, Tổ thẩm định thuộc Bộ Y tế và cá nhân các chuyên gia thẩm định trực tiếp chịu trách nhiệm về những thiếu sót, vi phạm trong việc thẩm định, xét duyệt cấp số đăng ký đối với 07 thuốc, cấp phép nhập khẩu đối với 03 thuốc và cấp phép hoạt động về thuốc và nguyên liệu làm thuốc tại Việt Nam cho Công ty Helix.
Không có sự “ưu ái” về thời hạn trong cấp phép nhập khẩu và cấp giấy đăng ký lưu hành
Một trong những yêu cầu của Thủ tướng Chính phủ là làm rõ việc cấp phép nhập khẩu thuốc và cấp giấy đăng ký lưu hành thuốc đối với 10 loại thuốc (thuốc) do Công ty Helix Pharmaceuticals Inc., Canada sản xuất, trong đó: cấp giấy đăng ký lưu hành 07 thuốc và cấp giấy phép nhập khẩu 3 thuốc; cấp giấy phép hoạt động về thuốc và nguyên liệu làm thuốc tại Việt Nam cho Công ty Helix đã được Thanh tra Chính phủ làm rõ trong kết luận.
Theo kết luận, thời gian thẩm định và cấp số đăng ký đối với 07 thuốc chậm so với quy định từ 100 đến 150 ngày; Thời hạn xét duyệt, cấp giấy phép nhập khẩu 03 thuốc chậm từ 28 đến 60 ngày; Thời hạn xét duyệt cấp giấy phép hoạt động chậm 53 ngày. Thanh tra Chính phủ khẳng định việc chậm này là vi phạm quy định và trách nhiệm thuộc về các thành viên của Tổ chuyên gia thẩm định.
Nguyễn Hùng