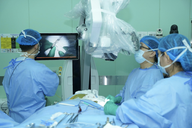
Bộ trưởng Y tế lần đầu trả lời về việc tạm ngừng vắc xin Quinvaxem
(Dân trí) - Hơn 1 tháng kể từ ngày Bộ Y tế bất ngờ ra thông báo khẩn tạm dừng sử dụng vắc xin Quinvaxem trong chương trình tiêm chủng mở rộng (TCMR) trên toàn quốc (hôm 4/5), Bộ trưởng Bộ Y tế lần đầu lên tiếng về việc tạm dừng loại vắc xin này.
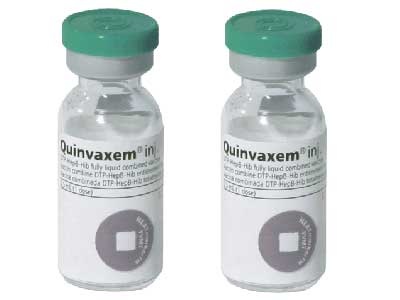
Thuốc, vắc xin đều có phản ứng không mong muốn
Theo Bộ trưởng Bộ Y tế Nguyễn Thị Kim Tiến, thuốc và vắc-xin khi sử dụng đều có phản ứng bất lợi không mong muốn. Vắc-xin có chứa kháng nguyên, khi tiêm có thể xảy ra các trường hợp phản ứng sau tiêm chủng từ nhẹ đến nặng và có thể gây tử vong đối với cá nhân có cơ địa mẫn cảm.
Theo báo cáo của Tổ chức Y tế thế giới, tỷ lệ phản ứng nặng sau tiêm chủng/1 triệu liều vắc-xin sử dụng đối với từng loại như sau: vắc-xin Bạch hầu - Ho gà - Uốn ván là 20 trường hợp/1 triệu liều sử dụng, Bại liệt là 1-3 trường hợp/1triệu liều, Viêm gan B từ 1-2 trường hợp/1 triệu liều, Sởi là 1-50 trường hợp/1 triệu liều, Uốn ván từ 1- 6 trường hợp/1 triệu liều. Một số nước trên thế giới khi sử dụng Quinvaxem đã có báo cáo phản ứng nặng khi tiêm như Srilanka, Butan, Pakistan, Brasil, Philippine... trong hơn 90 nước sử dụng có Srilanka, Butan đã tạm dừng sử dụng Quinvaxem một thời gian do nghi ngờ xảy ra tai biến khi tiêm, sau đó đã tiếp tục sử dụng lại.
Tại Việt Nam, 3 tháng đầu năm 2013, toàn quốc ghi nhận 5 trường hợp tử vong sau tiêm. Theo kết luận của Hội đồng tư vấn chuyên môn đánh giá tai biến trong quá trình sử dụng vắc-xin, sinh phẩm y tế, trong số 5 trường hợp tử vong nêu trên có 4 trường hợp không liên quan đến tiêm chủng và chất lượng vắc-xin, 1 trường hợp chưa chẩn đoán được nguyên nhân tử vong.
“Mặc dù chưa có bằng chứng chứng minh các trường hợp tử vong có liên quan đến vắc-xin, các trường hợp tử vong trên có thể là sự trùng hợp vì tỷ lệ tử vong của trẻ dưới 1 tuổi tại Việt Nam là 15,8 %o, hoặc do các bệnh khác như viêm phổi, tim mạch,… nhưng để thận trọng hơn và đảm bảo an toàn tối đa cho tiêm chủng, Bộ Y tế quyết định tạm dừng sử dụng vắc-xin Quinvaxem (dự kiến trong khoảng 3 tháng) để các cơ quan chuyên môn phối hợp với Tổ chức Y tế thế giới, Quỹ nhi đồng liên hợp quốc và các nhà khoa học khác trên thế giới tiến hành đánh giá tổng thể về vắc-xin này ở Việt Nam và gửi các lô vắc-xin sang phòng kiểm định độc lập tại nước Anh để kiểm định lại chất lượng vắc-xin”, bà Tiến khẳng định.
400 triệu liều Quinvaxem đã được sử dụng
Vắc xin Quinvaxem do công ty Berna Biotech, Hàn Quốc sản xuất để phòng 5 bệnh truyền nhiễm nguy hiểm là Bạch hầu, Ho gà, Uốn ván, Viêm gan B, Viêm màng não mủ, viêm phổi (Hib). Vắc xin này có chứa thành phần kháng nguyên ho gà toàn tế bào (một số nước phát triển có điều kiện kinh tế như Mỹ, Nhật Bản, Hàn Quốc sử dụng vắc xin có chứa kháng nguyên ho gà vô bào nên ít tai biến hơn).
Trước khi nhận tài trợ của GAVI để đưa vắc xin này vào Việt Nam (năm 2010), vắc xin Quinvaxem đã được Tổ chức Y tế thế giới tiền thẩm định về chất lượng vào tháng 9 năm 2006 và đã được sử dụng ở hơn 90 nước trên thế giới với tổng số hơn 400 triệu liều đã được sử dụng.
Sau khi thực hiện quy trình đánh giá về hiệu lực và an toàn của vắc-xin tại Việt Nam, năm 2010 Bộ Y tế đã đưa Quinvaxem vào sử dụng tại Việt Nam. Tổng số liều đã nhận từ viện trợ là khoảng 16,2 triệu, trong đó đã cấp phát 15,2 triệu liều, chiếm 4,1% so với số liều mà các nước trên thế giới đã sử dụng.
Theo nữ Bộ trưởng này, việc tạm dừng sử dụng vắc xin là một thực hành thông thường trong chương trình tiêm chủng mở rộng. Trước đây vào năm 2012, Bộ Y tế đã cho tạm dừng sử dụng một lô vắc-xin Quinvaxem trên phạm vi toàn quốc do nghi ngờ vắc-xin có liên quan đến phản ứng nặng sau tiêm. Thời gian tạm dừng sử dụng trong 1-3 tháng không ảnh hưởng đến đáp ứng miễn dịch của trẻ.
Dự kiến cuối tháng 6/2013 chúng ta sẽ có đầy đủ kết luận về tính an toàn của vắc xin Quinvaxem của Tổ chức Y tế thế giới. Khi đó, Bộ Y tế sẽ đưa ra quyết định dùng lại vắc xin này hay thay thế bằng một vắc xin khác. Tại cuộc họp toàn cầu về an toàn tiêm chủng chắp tới đây, Bộ Y tế cũng sẽ tham gia, trong đó có xem xét vấn đề về vắc-xin Quinvaxem. Nếu xác định chất lượng vắc-xin Quinvaxem không phải nguyên nhân gây ra các trường hợp phản ứng nặng sau tiêm chủng, Bộ Y tế sẽ chỉ đạo các địa phương tiếp tục sử dụng vắc-xin này. Trường hợp xác định nguyên nhân do vắc-xin Quinvaxem thì sẽ sử dụng vắc-xin khác thay thế.
Theo bà Tiến, khi đưa ra quyết định tạm dừng sử dụng vắc xin Quinvaxem trên toàn quốc để đánh giá, kiểm định lại chất lượng vắc xin, Bộ Y tế cũng đã xây dựng đề án thay thế vắc xin toàn tế bào bằng vắc-xin vô bào trình Chính phủ.
“Tuy nhiên, không có vắc-xin nào là tuyệt đối an toàn, kể cả việc thay thế bằng vắc-xin vô bào vẫn có thể xảy ra các trường hợp tai biến”, bà Tiến nói.
Trong thời gian tạm dừng vắc-xin Quinvaxem, Bộ Y tế đã hướng dẫn các cơ sở y tế tư vấn, cung cấp thông tin cho các bà mẹ về việc tạm dừng tiêm không ảnh hưởng đến sinh miễn dịch của trẻ, triển khai kế hoạch tăng cường công tác bảo đảm an toàn tiêm chủng và triển khai tập huấn bổ sung cho các cán bộ y tế về tiêm chủng an toàn nhằm nâng cao năng lực thực hành của cán bộ tiêm chủng.
Hồng Hải