Trước khi xin cấp phép khẩn cấp, kết quả thử nghiệm của Nanocovax ra sao?
(Dân trí) - Đến thời điểm hiện tại, Nanocovax của Công ty Nanogen là vắc xin Covid-19 đầu tiên và duy nhất của Việt Nam bước sang giai đoạn thử nghiệm lâm sàng thứ 3.
Kết quả thử nghiệm lâm sàng vắc xin Nanocovax
Từ tháng 4/2020, Công ty Nanogen đã bắt tay tìm hiểu nghiên cứu thuốc và vắc xin ngừa virus SARS-CoV-2. Đến giữa tháng 12/2020, sau nghiên cứu, sản xuất và thử hàng loạt trên động vật thành công, Bộ Y tế chính thức bấm nút cho phép thử nghiệm vắc xin ngừa Covid-19 do Nanogen sản xuất trên người giai đoạn một.
Vắc xin Nanocovax.
Giai đoạn một: Nanocovax đạt độ an toàn 100%
Ngày 8/2, Nanocovax hoàn thành 120 mũi tiêm thử nghiệm lâm sàng giai đoạn một trên 60 tình nguyện viên. Theo đại diện nhóm nghiên cứu, cả 3 liều tiêm 25mcg, 50mcg và 75mcg có độ an toàn đạt 100%, hiệu quả bảo vệ người tiêm không bị nhiễm virus SARS-CoV-2 lên đến 90% và tất cả đều sinh miễn dịch tốt. Hầu hết các tình nguyện viên đều có sức khỏe ổn định sau tiêm. Một số ít trường hợp có biểu hiện đau tại vị trí tiêm, sốt nhẹ, nhưng đều hết sau ít ngày.
Tiêm thử nghiệm vắc xin Nanocovax.
Giai đoạn 2: Tính sinh miễn dịch của Nanocovax lên đến 99,4%
Kết quả thử nghiệm lâm sàng giai đoạn 2 cho thấy, vắc xin Nanocovax an toàn, 100% tình nguyện viên đều sinh miễn dịch, tỉ lệ chuyển đổi huyết thanh đạt đến 99,4% và kháng thể sinh ra có thể chống lại virus chủng Vũ Hán và các biến chủng mới. Các phản ứng phụ của Nanocovax thậm chí còn thấp hơn Pfizer và Moderna, chưa ghi nhận trường hợp nào sốc phản vệ, các trường hợp có sốt đều rất nhẹ từ 37,5-38 độ C và tự hết.
Giai đoạn 3: Thử nghiệm trên 13.000 người
Dựa trên kết quả rất tốt của giai đoạn một và giai đoạn 2, trưa 11/6, Bộ Y tế chính thức phê duyệt đề cương thử nghiệm giai đoạn 3 vắc xin Nanocovax (liều 25 mcg). Giai đoạn 3 sẽ được thử nghiệm trên 13.000 tình nguyện viên. 2 nghiên cứu viên chính của giai đoạn này là Học Viện Quân y (Hà Nội) và Viện Pasteur TPHCM ở Miền Nam. Hiện tại, 1.000 tình nguyện viên đã hoàn thành mũi tiêm thứ nhất.
TS Hồ Nhân, Tổng giám đốc Công ty Nanogen thông tin, đơn vị này cũng đã gửi mẫu huyết thanh của các tình nguyện viên đã tiêm vắc xin Nanocovax đến các cơ sở nghiên cứu trong nước, để đánh giá khả năng trung hòa biến chủng Delta (biến chủng Ấn Độ).
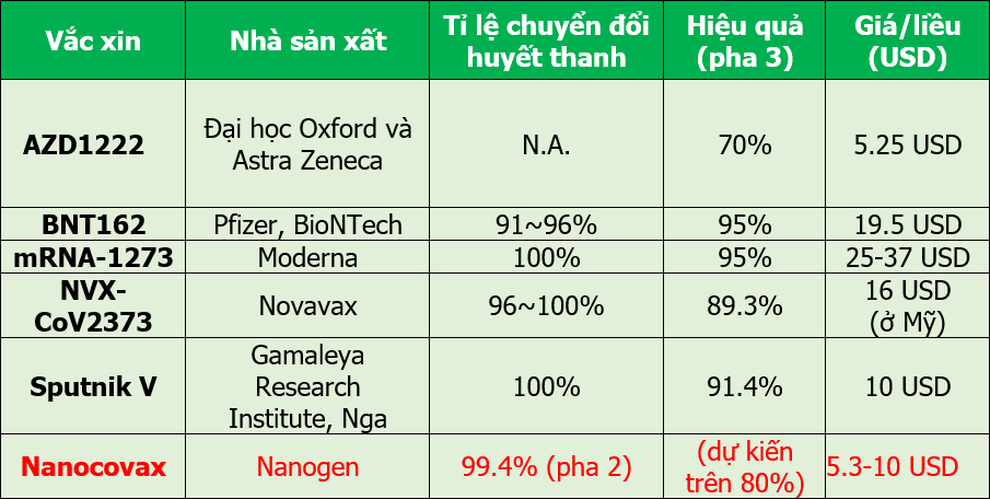
So sánh hiệu quả bảo vệ của vắc xin Nanocovax và các loại vắc xin Covid-19 trên thế giới (Nguồn: Nanogen).
Theo Nanogen, các kết quả thu được đến thời điểm hiện tại cho thấy Nanocovax có độ an toàn và khả năng sinh miễn dịch không kém các vắc xin Covid-19 đang được lưu hành trên thế giới. Tuy nhiên, nhờ sử dụng công nghệ mà công ty đã làm chủ được trong hơn 10 năm nay và đảm bảo được nguồn nguyên liệu tốt nên giá bán dự kiến của Nanocovax hiện nay là 120.000 đồng/liều (thấp nhất thế giới).
Cần thêm ít nhất 2 tháng để đánh giá hiệu lực bảo vệ của Nanocovax
Theo thông tin của Tổ chức Y tế thế giới (WHO), đến ngày 6/4, có 269 vắc xin Covid-19 đang triển khai nghiên cứu trên toàn thế giới, trong đó có 85 vắc xin đang trong quá trình thử nghiệm lâm sàng (15 vắc xin thử nghiệm lâm sàng giai đoạn 3), 184 loại đang trong quá trình nghiên cứu tiền lâm sàng.
Về cơ bản, các vắc xin phòng Covid-19 của các hãng trên thế hiện nay đang có đều được cấp phép trong tình trạng khẩn cấp.
Theo quy định của Tổ chức Y tế Thế giới, vắc xin trước khi đưa vào sử dụng khẩn cấp bắt buộc phải thử nghiệm lâm sàng trên người với 3 giai đoạn, trong đó giai đoạn 3 là quan trọng nhất.
Trao đổi với PV Dân trí chiều 22/6, TS Hồ Nhân cho biết, đơn vị này đã có văn bản gửi Thủ tướng Chính phủ về việc xin cấp phép khẩn cấp vắc xin Covid-19 Nanocovax.
Cụ thể, trong văn bản, Nanogen bày tỏ mong muốn vắc xin Nanocovax sớm được cấp phép khẩn cấp có điều kiện, tương tự như các loại vắc xin của Nga, Trung Quốc và Ấn Độ.
Về việc cấp phép khẩn cấp vắc xin Covid-19, ông Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học Công nghệ và Đào tạo, Bộ Y tế cho hay, trong bối cảnh hiện nay, việc cấp phép khẩn cấp cho một loại vắc xin phòng Covid-19 là điều cần thiết, tuy nhiên tất cả phải trên nguyên tắc đầy đủ các dữ liệu về mặt khoa học. Cụ thể, phải chứng minh và trả lời được 3 câu hỏi lớn là: Có an toàn không? Có sinh miễn dịch không? Và điều đặc biệt quan trọng đó là có hiệu lực bảo vệ không?

Ông Nguyễn Ngô Quang, Phó cục trưởng Cục Khoa học - Công nghệ và Đào tạo (Bộ Y tế).
Vắc xin Nanocovax đang thử nghiệm giai đoạn 3 trên 1.000 người. Theo ông Quang, đây là số lượng nhỏ, chưa mang tính cộng đồng, chưa nói lên nhiều so với số lượng hàng trăm triệu người sẽ sử dụng vắc xin sau này. Song việc xem xét cấp phép khẩn cấp là phương án được cân nhắc trong trường hợp dịch bệnh khẩn cấp.
Theo ông Quang, các dữ liệu hiện tại cho thấy vắc xin Nanocovax an toàn, có tính sinh miễn dịch nhưng hiệu lực bảo vệ như thế nào vẫn đang trong thời gian nghiên cứu, thử nghiệm tiếp. Để có đủ căn cứ khoa học đánh giá cần phải theo dõi sau tiêm mũi một 36 ngày, 45 ngày và 56 ngày, từ đó mới đủ tiêu chuẩn để đánh giá tính sinh miễn dịch và hiệu lực bảo vệ. Vì thế, cần ít nhất 2 tháng nữa mới có thể đánh giá được.










