Chuyên gia nói gì về việc gia hạn sử dụng vaccine Pfizer từ 6 lên 9 tháng?
(Dân trí) - TS Phạm Quang Thái cho biết việc gia hạn sử dụng vaccine không phải là tình huống đầu tiên và cũng không phải là không có tiền lệ. Quyết định này dựa trên các cơ sở khoa học là nghiên cứu của hãng.
Liên quan đến việc Việt Nam cho phép gia hạn sử dụng đối với 2 lô vaccine Pfizer, TS Phạm Quang Thái, Trưởng văn phòng Tiêm chủng mở rộng miền Bắc, Viện Vệ sinh dịch tễ Trung ương cho biết đây không phải là tình huống đầu tiên và cũng không phải là một vấn đề không có tiền lệ. Vì tất cả các vaccine đều có hiện tượng này cũng tương tự như thuốc cũng có thời điểm người ta quy định gia hạn một loại vaccine, một loại thuốc nào đó.
Lý do là vì một sản phẩm sau khi được tạo ra thì bao giờ nhà sản xuất cũng đánh giá xem độ bền của sản phẩm với nhiệt độ như thế nào. Đây là điều hết sức quan trọng vì nếu như không đánh giá được độ bền của một sản phẩm với vấn đề bảo quản thì sẽ không thể đảm bảo đóng hạn sử dụng chính xác.

TS Phạm Quang Thái, Trưởng văn phòng Tiêm chủng mở rộng miền Bắc, Viện Vệ sinh dịch tễ Trung ương (Ảnh: Tuấn Mark).
Theo đó, dựa vào cơ sở khoa học là các nghiên cứu trước đây, hãng quy định hạn sử dụng của vaccine là 6 tháng. Tuy nhiên, trong quá trình sử dụng, bảo quản của loại vaccine này, với mỗi lô hãng sẽ giữ lại một lượng vaccine nhất định, bảo quản trong điều kiện tiêu chuẩn, ở đây là âm 60 đến âm 90 độ C. Với điều kiện bảo quản như vậy, theo thời gian hãng sẽ đánh giá lại về hiệu lực, độ bền.
"Người ta thấy 6 tháng, 9 tháng thì sản phẩm vẫn có chất lượng như ban đầu, tức là vẫn đảm bảo tính sinh miễn dịch, vẫn đảm bảo về các thông tin về hóa lý, cảm quan và đặc biệt vẫn đảm bảo các vấn đề về an toàn. Với các cơ sở khoa học như vậy, hãng sẽ đệ đơn lên một cơ quan trọng tài cao nhất là FDA của Hoa Kỳ, để xin hạn dùng là 9 tháng thay vì 6 tháng. Với cơ sở đề xuất của hãng, FDA căn cứ theo bằng chứng thực tế, sẽ quyết định gia hạn", TS Thái lý giải.
Nhiều nước đã chấp nhận gia hạn sử dụng vaccine của Pfizer
Tại thời điểm ngày 24/8, FDA đã gia hạn cho tất cả các lô vaccine của Pfizer nếu bảo quản ở điều kiện chuẩn từ âm 60 đến âm 90 độ C thì sẽ được gia hạn tự động từ 6 tháng lên 9 tháng. Đấy là cơ sở về mặt khoa học, pháp lý cho việc gia hạn.
Cũng theo chuyên gia, khi nhập vaccine về, Việt Nam cũng phải căn cứ trên các cơ sở pháp lý như vậy. Khi hãng đưa các cơ sở pháp lý như thế thì lô vaccine về cũng sẽ được gia hạn theo quy định của nhà sản xuất.
Khi nộp hồ sơ cho phía Việt Nam, nhà sản xuất ghi hạn sử dụng là tháng 11/2021. Vì thế, hãng phải có văn bản lên Cục Quản lý Dược và Bộ Y tế xin phép theo hạn đã được phê duyệt tại Mỹ. Trên cơ sở các bằng chứng như vậy, Bộ Y tế Việt Nam đã quyết định đồng ý theo đề xuất, cơ sở pháp lý của hãng đưa ra.
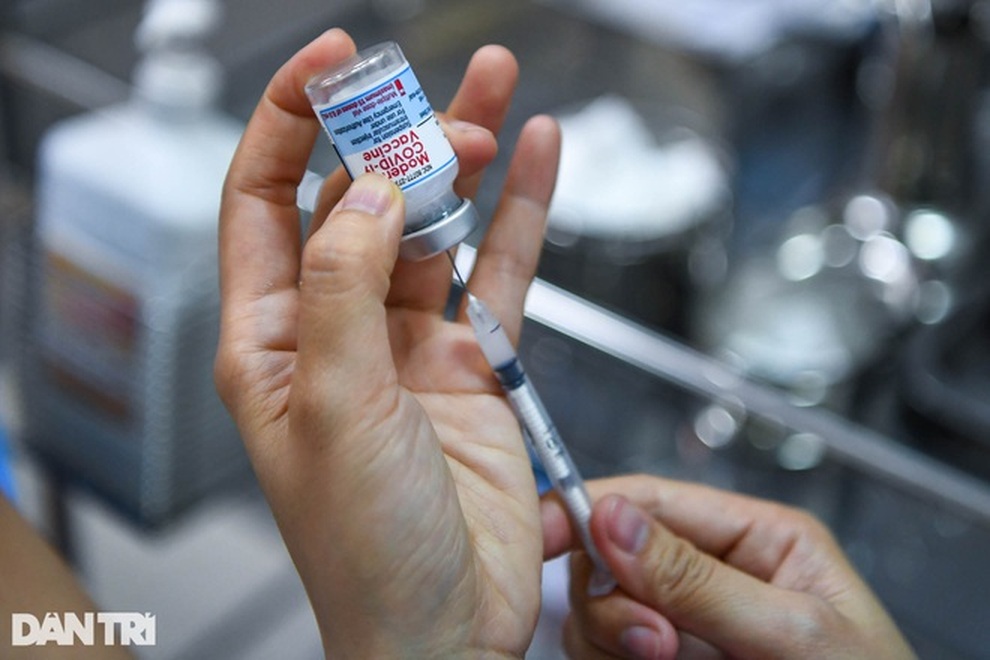
Không chỉ với Việt Nam mà với tất cả các thị trường, hãng cũng phải chuyển tất cả các bằng chứng khoa học liên quan. FDA Hoa Kỳ, cơ quan quản lý Dược của châu Âu cũng chấp nhận việc gia hạn từ 6 tháng lên 9 tháng của Pfizer. Các quốc gia khác như Anh, Nhật… cũng đều nhận được thông báo của hãng liên quan đến việc tăng hạn sử dụng.
Thực tế, hiện nay các nước đều căn cứ trên cơ sở pháp lý của nhà sản xuất và sự phê duyệt của cơ quan quản lý quốc gia để ra quyết định tiếp tục sử dụng và khi đã tiếp tục sử dụng thì không có vấn đề gì về mặt khoa học hay an toàn.
"Vaccine khi về đến Việt Nam cũng như được lưu trữ tại Viện, trong suốt quá trình vận chuyển thì đều được bảo quản trong điều kiện âm sâu, trong phạm vi âm 60 đến âm 90 độ. Đây là điều kiện bảo quản lý tưởng để giữ được vaccine trong khoảng thời gian 9 tháng kể từ ngày sản xuất và chỉ khi chuyển xuống để sử dụng tại thực địa thì vaccine đó mới đã được rã băng", TS Thái cho biết.
Tại thời điểm rã băng, vaccine còn tiếp tục được sử dụng một tháng nữa thì mới thể được tính hết hạn sử dụng đối với lô vaccine đã rã băng. Với cách bảo quản chặt chẽ như vậy thì vaccine sẽ đảm bảo chất lượng như khuyến cáo của nhà sản xuất.
Trong văn bản của Cục Quản lý Dược cũng nêu rõ với sự điều chỉnh của hãng thì hãng sẽ chịu trách nhiệm nếu xảy ra các vấn đề liên quan đến chất lượng.
Trong quá trình vaccine lưu hành, Viện Kiểm định Vaccine và sinh phẩm quốc gia của Việt Nam cũng là đơn vị độc lập để đánh giá vaccine đang lưu hành đó xem có bất kỳ biến đổi về mặt cảm quan, lý tính, yếu tố liên quan hiệu lực bảo vệ của vaccine hay không, từ đó đưa ra các khuyến cáo kịp thời nếu như có bất cứ vấn đề gì quan ngại.
Về thay đổi nhãn của vaccine, theo TS Thái, với những loại vaccine bảo quản ở 2-8 độ C và các sản phẩm thuốc thông thường bảo quản 25 độ thì việc dán nhãn lại, rồi đánh dấu dập lại thời điểm hết hạn rất dễ dàng. Thay vì mỗi quyết định bằng văn bản nhà sản xuất có thể điều chỉnh lại nhãn để tránh hiểu lầm liên quan đến người sử dụng.
Tuy nhiên với loại nhãn hết sức đặc biệt là nhãn có thể chịu được nhiệt độ đông băng như nhãn sử dụng với vaccine Pfizer thì việc dán lại là hoàn toàn không khả thi cũng như vấn đề in lại thông tin về hạn sử dụng lên nhãn cũng không khả thi. Vì thế, chúng ta chỉ điều chỉnh bằng văn bản, không điều chỉnh nhãn được. Chính vì vậy, có sự hiểu lầm từ phía người sử dụng là các phụ huynh trong thời gian vừa rồi.
"Đây là việc hết sức đáng tiếc. Chúng tôi hy vọng rằng với những sự giải thích mang tính chất khoa học và chuyên môn có thể giúp cho các phụ huynh yên tâm và tuân thủ hướng dẫn của y bác sĩ để có thể tiếp tục sử dụng vaccine và theo dõi sức khỏe của trẻ cẩn trọng hơn", TS Thái nhấn mạnh.