Đại học Quốc gia Hà Nội làm chủ được công nghệ nền để sản xuất vắc xin mARN
(Dân trí) - Nhóm nghiên cứu liên ngành Sinh-Y-Dược của Trường Đại học Y Dược và Tin-Sinh tại Trường Đại học Công nghệ (ĐHQGHN) đã hoàn thành việc thiết lập công nghệ nền sản xuất vắc xin mARN.
PGS.TS. Đinh Đoàn Long - Phó Hiệu trưởng Trường ĐH Y Dược, ĐHQGHN cho biết: Trong phần lớn thế kỷ XX, việc điều chế văcxin chủ yếu dựa trên 2 công nghệ chính là Vắc xin virus sống giảm độc lực và Vắc xin virus bất hoạt. Cả hai công nghệ này đều có bước nuôi và sản xuất virus trong điều kiện nghiêm ngặt, sau đó làm suy yếu hoặc gây chết chúng.

PGS.TS. Đinh Đoàn Long - Phó Hiệu trưởng Trường ĐH Y Dược, ĐHQGHN.
Đến cuối thế kỷ XX, nhờ sự phát triển của công nghệ sinh học phân tử - tế bào, công nghệ vắc xin protein kháng nguyên bề mặt virus ra đời. Thành phần vắc xin lúc này chỉ mang một số phân đoạn protein bề mặt (lớp áo) của virus.
Mỗi khi được tiêm, những phân đoạn protein này sẽ "dạy" cơ thể cách nhận diện các virus nguyên vẹn giống như cách chúng ta dùng "dấu vân tay" trên chứng minh thư để nhận diện mỗi cá thể. Các công nghệ vắc xin trên đến nay được coi là truyền thống có điểm chung là dùng thành phần protein bề mặt virus giả lập quá trình lây nhiễm tự nhiên.
Ưu điểm của các công nghệ này hiện nay là ở nhiều quốc gia đã sẵn có các dây chuyền sản xuất, đã quen các quy trình quản lý, vận hành theo tiêu chuẩn ngành dược (GPP, GMP). Nhưng nhược điểm của các công nghệ truyền thống là thời gian phát triển vắc xin mới thường kéo dài. Đối với mỗi biến chủng cần ít nhất nhiều tháng thậm chí nhiều năm để phát triển được vắc xin đặc hiệu. Trong quy trình sản xuất vắc xin có bước sản xuất và tinh sạch protein kháng nguyên được coi là nghiêm ngặt, phức tạp, cần thời gian dài mỗi khi cần mở rộng sản xuất nhằm nâng cao sản lượng.
Đầu thế kỷ XXI, công nghệ sản xuất vắc xin có bước ngoặt lớn với sự ra đời của các vắc xin axit nucleic (mARN và ADN). Công nghệ vắc xin axit nucleic có đặc trưng là bỏ qua bước tổng hợp và tinh sạch protein kháng nguyên bề mặt virus, mà thay vào đó lợi dụng chính các tế bào người được tiêm vắc xin làm "nhà máy" để tự sản sinh các protein kháng nguyên này (bắt chước cơ chế trình diện kháng nguyên tự nhiên của hệ miễn dịch), qua đó giúp đáp ứng miễn dịch diễn ra nhanh, hiệu quả cao.
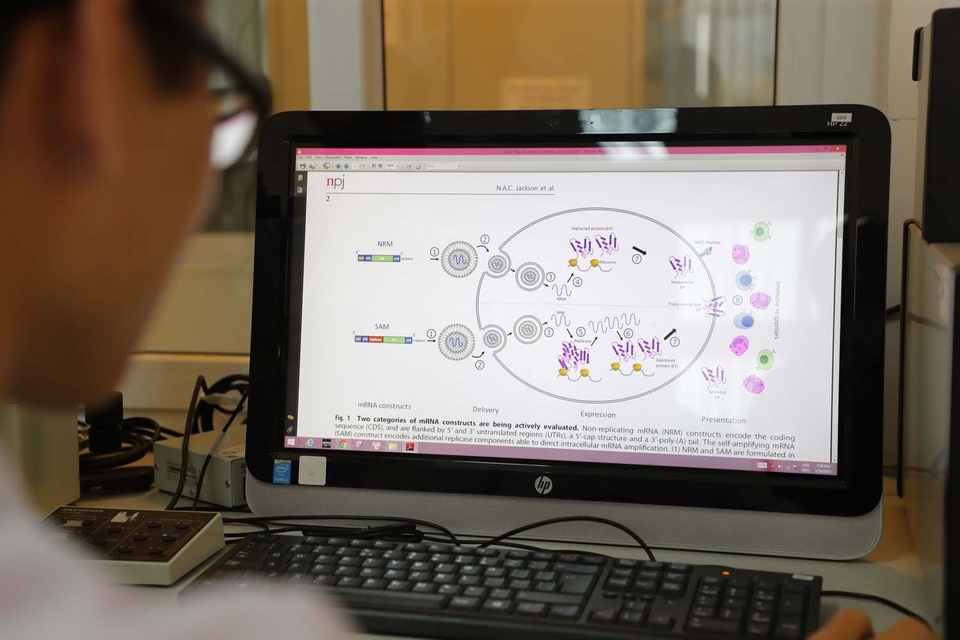
Nhờ công nghệ vắc xin axit nucleic, thời gian phát triển vắc xin mới được rút ngắn đáng kể.
Ưu điểm nổi trội của công nghệ vắc xin mARN và ADN này là thời gian nghiên cứu và phát triển vắc xin được rút ngắn đáng kể, nhất là khi có sự phối hợp của công nghệ tin-miễn dịch (immunoformatics) và công nghệ ADN tái tổ hợp (recombinant DNA technology) cho phép sàng lọc, dự đoán và sản xuất nhanh các trình tự mARN và ADN mã hóa kháng nguyên của các biến chủng mới. Nhờ vậy, với mỗi biến thể virus, có thể phát triển được vắc xin đặc hiệu sẵn sàng cho thử nghiệm dược lý chỉ trong vài tuần. Như vậy sẽ rút ngắn được thời gian nghiên cứu phát triển vắc xin mới nhiều lần về thời gian. Ngoài công nghệ tin-miễn dịch, sự thành công của các văcxin axit nucleic gần đây còn nhờ các công nghệ phụ trợ như công nghệ vật liệu nano giúp bọc và mang các phân tử mARN và ADN vượt hàng rào miễn dịch tới các tế bào đích của cơ thể.
Các vắc xin phòng chống Covid-19 được cấp phép và sử dụng rộng rãi nhất hiện nay trên thế giới phản ánh đầy đủ các công nghệ sản xuất vắc xin hiện có, như vắc xin mARN (của Moderna và Pfizer), vắc xin ADN (của AstraZeneca, Johnson & Johnson), vắc xin protein kháng nguyên bề mặt virus (Sputnik V của Nga) hay vắc xin virus bất hoạt (Sinovax của Trung Quốc). Trong đó, đây là lần đầu tiên trên thế giới, các vắc xin axit nucleic được cấp phép và đưa vào tiêm chủng đại trà. Ngược lại, cũng nhờ công nghệ vắc xin axit nucleic, thời gian phát triển vắc xin mới được rút ngắn đáng kể.
Để phát triển vắc xin axit nucleic cần có công nghệ nền tương ứng với 4 bước của quá trình sản xuất: Bước 1 là công nghệ Tin-Sinh (tin - miễn dịch) giúp sàng lọc và dự đoán nhanh các trình tự gen và/hoặc mARN mã kháng nguyên đặc hiệu virus và các biến chủng của chúng; Bước 2 là công nghệ ADN tái tổ hợp để tạo các cấu trúc vectơ làm khuôn tổng hợp nhanh các mARN/ADN hiệu suất cao. Đây bản chất là một "cỗ máy phân tử" cho phép tổng hợp bất cứ phân tử mARN/ADN ứng viên nào mỗi khi được công nghệ tin-miễn dịch tìm ra; Bước 3 là công nghệ tổng hợp axit nucleic không dùng tế bào giúp dễ dàng mở rộng quy mô sản xuất và biến đổi hóa học axit nucleic vượt qua các hàng rào miễn dịch tự nhiên nhằm nâng cao hiệu quả của vắc xin; Cuối cùng (Bước 4) là công nghệ tinh sạch và bao gói axit nucleic làm vắc xin thành phẩm.
Trong 4 bước trên thì bước 4 là một quy trình được chuẩn hóa, về nguyên tắc, có thể áp dụng cho mọi sản phẩm mARN. Ba bước đầu tiên là công nghệ nền giúp đáp ứng nhanh với các biến chủng.

"Đến nay, tại ĐHQGHN nhóm nghiên cứu liên ngành Sinh-Y-Dược tại Trường Đại học Y Dược và Tin-Sinh tại Trường Đại học Công nghệ đã hoàn thành việc thiết lập các công nghệ nền này, xuất phát từ "cỗ máy phân tử" có nguồn gốc từ adenovirut và alphavirut (nhưng đã được làm mất hoàn toàn hoạt động sống của virus); tình cờ đây cũng là hệ thống tương tự được các hãng Pfizer, Moderna, AstraZeneca, Johnson&Johnson sử dụng cho phát triển và sản xuất các vắc xin axit nucleic của họ theo các báo cáo chúng tôi thu thập được", PGS.TS. Đinh Đoàn Long thông tin.
Cũng theo PGS Long, nhóm nghiên cứu sẽ tập trung ứng dụng 4 công nghệ nền theo các công đoạn của quá trình phát triển và thử nghiệm vắc xin mARN gồm: tin - miễn dịch, công nghệ ADN tái tổ hợp, công nghệ tổng hợp và bọc hệ mang mARN/ADN đối với một số biến thể Covid-19 được phân lập và báo cáo xuất hiện ở Việt Nam và thử nghiệm trên mô hình động vật thí nghiệm tuân thủ các yêu cầu về phát triển và thử nghiệm vắc xin của Tổ chức Y tế Thế giới (WHO) và của Bộ Y tế Việt Nam.
"Nhóm nghiên cứu tại Đại học Quốc gia Hà Nội không đầu tư cho bước sản xuất thử nghiệm mà sẽ chuyển giao cho các doanh nghiệp có kinh nghiệm sản xuất trong lĩnh vực này để quá trình nghiên cứu, phát triển vắc xin của cả hệ thống trong nước được rút ngắn, tiết kiệm và hiệu quả", PGS.TS Long chia sẻ.





